Khi nói đến việc tạo ra vắc-xin hoặc liệu pháp dựa trên mRNA, bạn nên bắt đầu theo cách bạn muốn kết thúc — với hiệu suất tối ưu. Bước đầu tiên của quá trình phiên mã in vitro (IVT) là lựa chọn enzyme cắt giới hạn (RE) phù hợp nhất để tuyến tính hóa khuôn IVT, chẳng hạn như plasmid, nhằm phục vụ cho phiên mã dạng run-off. Trong bài viết này, chúng tôi trình bày các yếu tố thực tiễn cần cân nhắc khi lựa chọn enzyme cắt giới hạn cho IVT.
Đại dịch COVID-19 đã đòi hỏi việc phát triển vắc-xin với tốc độ kỷ lục, và các vắc-xin dựa trên mRNA đã nổi lên như những lựa chọn thay thế cho các phương pháp truyền thống. Sự biểu hiện của mRNA có tính tạm thời và nhanh chóng. mRNA cũng dễ tổng hợp, tiêu chuẩn hóa và mở rộng quy mô — những đặc điểm này giúp đơn giản hóa đáng kể các giai đoạn nghiên cứu khám phá và phát triển ban đầu. Ngay sau khi giải trình tự bộ gen virus, trình tự DNA mục tiêu (có thể dùng làm kháng nguyên vắc-xin) có thể được xác định chỉ trong vài ngày. Đây là một thành tựu khoa học đáng chú ý và hiện đang được áp dụng cho nhiều loại virus khác như bệnh dại, cúm và RSV.
Những lợi thế tương tự cũng được áp dụng trong các lĩnh vực điều trị khác. Đặc biệt, các liệu pháp cá thể hóa “thiết kế riêng” hiện đã trở thành hiện thực. Vào đầu năm 2025, bé KJ (Muldoon) đã trở thành người đầu tiên trên thế giới được điều trị bằng liệu pháp CRISPR cá thể hóa, sử dụng mRNA để điều trị một rối loạn di truyền hiếm gặp đe dọa tính mạng. Các liệu pháp cá thể hóa cũng đang được ứng dụng trong điều trị ung thư, trong đó mRNA mã hóa các kháng nguyên liên quan đến ung thư nhằm kích hoạt hệ miễn dịch tấn công các tế bào ác tính.
Con đường enzyme từ khuôn DNA đến mRNA chức năng
Quy trình tạo vắc-xin hoặc liệu pháp mRNA sử dụng plasmid làm khuôn chủ yếu dựa trên các phản ứng enzyme: sau khi plasmid chứa trình tự mục tiêu được biến nạp vào vi khuẩn, nuôi cấy quy mô lớn và sau đó thu hoạch, tinh sạch, quy trình sẽ sử dụng nhiều loại enzyme khác nhau. Plasmid được tuyến tính hóa bằng enzyme cắt giới hạn, sau đó DNA này được dùng làm khuôn cho quá trình phiên mã in vitro để tạo mRNA.
Ngoài ra, để mRNA có chức năng và được bộ máy phiên mã của tế bào nhận diện, nó cần được gắn mũ (capping) đồng phiên mã hoặc bằng enzyme, cũng như có đuôi poly(A). mRNA thu được sau đó sẽ được phối trộn với các hạt nano lipid và đưa vào cơ thể dưới dạng mRNA đóng gói trong LNP.
Mặc dù quá trình tổng hợp mRNA in vitro đã tồn tại từ lâu và được ứng dụng rộng rãi trong công nghệ sinh học, phải đến năm 2012, mRNA tổng hợp mới được chứng minh là có khả năng kích thích đáp ứng miễn dịch, và đến năm 2017 mới được thử nghiệm làm vắc-xin chống lại virus Zika.
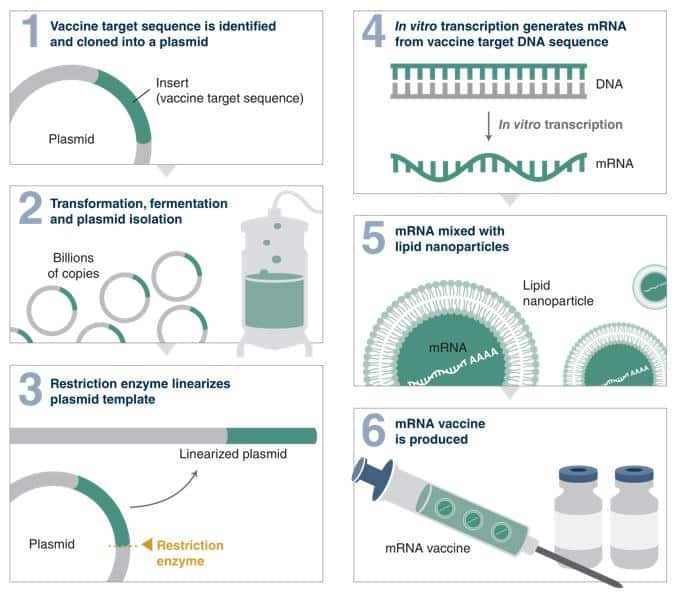
Ví dụ, một trong những bước quan trọng đầu tiên trong việc sản xuất vắc-xin SARS-CoV-2 là tuyến tính hóa DNA plasmid chứa gen mã hóa protein gai (spike) của virus. Các enzyme cắt giới hạn được sử dụng để tuyến tính hóa plasmid khuôn này. Vì vậy, cần đảm bảo rằng quá trình sản xuất và bào chế enzyme cắt giới hạn được thực hiện trong môi trường không có nguồn gốc động vật và tuân thủ các tiêu chuẩn chất lượng cao nhất.
NEB đã tham gia nghiên cứu và sản xuất enzyme cắt giới hạn trong hơn 50 năm – chuyên môn của chúng tôi trong lĩnh vực này cho phép cung cấp những hướng dẫn hữu ích khi lựa chọn enzyme cắt giới hạn cho phát triển liệu pháp mRNA:
Các yếu tố cần cân nhắc khi lựa chọn enzyme cắt giới hạn cho sản xuất mRNA
- Sản xuất không có nguồn gốc động vật giúp loại bỏ rủi ro: Các vật liệu có nguồn gốc động vật, như heparin, thường được sử dụng trong quá trình tinh sạch enzyme cắt giới hạn. NEB cung cấp các enzyme được xử lý và/hoặc bào chế mà không sử dụng sản phẩm từ động vật.
- Công thức không chứa thành phần từ động vật: Albumin, như BSA, thường được thêm vào để ổn định enzyme trong công thức cuối. NEB cung cấp các sản phẩm sử dụng albumin tái tổ hợp (rAlbumin), đảm bảo không có thành phần từ động vật, phù hợp với yêu cầu sản xuất theo tiêu chuẩn FDA.
- Trình tự nhận biết dài giúp giảm xử lý plasmid: Trình tự nhận biết càng dài thì khả năng xuất hiện trong đoạn gen càng thấp, từ đó đơn giản hóa việc thiết kế và sản xuất plasmid khuôn. Do đó, nên ưu tiên enzyme có trình tự nhận biết dài (7–8 base).
- Sản phẩm cắt DNA: Enzyme không nên tạo đầu nhô 3’. Sự hiện diện của đầu nhô 3’ có thể làm tăng các sản phẩm phụ không mong muốn, bao gồm RNA sợi đôi (dsRNA) trong quá trình phiên mã in vitro (IVT).
- Độ ổn định của enzyme để đạt hiệu suất tối ưu: Một số enzyme ổn định hơn các enzyme khác. Nên chọn enzyme có độ ổn định cao (ưu tiên hạn sử dụng 24 tháng và bảo quản ở -20°C). Cần lưu ý các enzyme có hạn dùng ngắn hơn hoặc yêu cầu bảo quản ở -80°C.
- Nhiệt độ ủ ảnh hưởng đến hoạt tính enzyme: Nhiệt độ ủ khuyến nghị cho đa số enzyme là 37°C, tuy nhiên một số enzyme cần nhiệt độ khác. Cần kiểm tra hoạt tính enzyme tại 37°C nếu thiết kế yêu cầu điều kiện cụ thể.
- Chất tẩy (detergent) phải tuân thủ quy định: Một số enzyme chứa lượng nhỏ chất tẩy (ví dụ Triton X-100) để tăng hoạt tính. Cần kiểm tra thành phần để đảm bảo phù hợp với quy định địa phương (ví dụ REACH tại châu Âu).
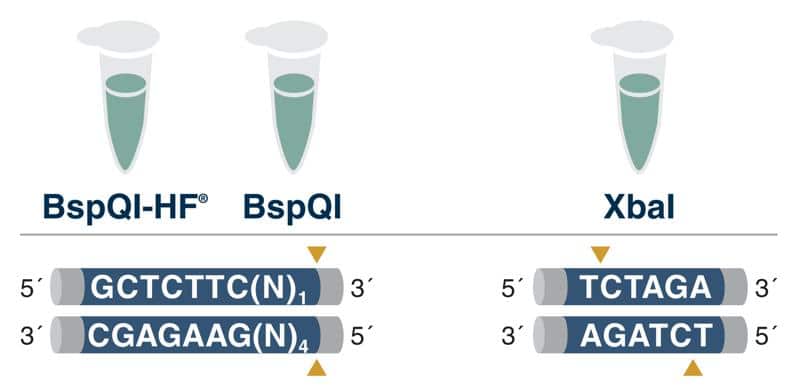
- Enzyme cắt giới hạn loại IIS cho khuôn “không để lại dấu vết” (scarless): Enzyme loại IIS cắt ngoài trình tự nhận biết, giúp bảo toàn tính toàn vẹn của đuôi poly(A) do nhà sản xuất thiết kế. Sau khi tuyến tính hóa, không để lại “dấu vết” trên DNA và không thêm nucleotide không mong muốn vào đầu 3’ của RNA.
- NEB cung cấp hơn 30 enzyme loại IIS: Bao gồm BspQI (isoschizomer của LguI và SapI) có sẵn ở cấp GMP, và BspQI-HF với nhiệt độ ủ 37°C.
- Enzyme yêu cầu nhiều vị trí cắt (multi-site): Một số enzyme cần nhiều hơn một vị trí nhận biết để cắt hiệu quả. Trong trường hợp này thường cần bổ sung oligo vào phản ứng, và sau đó phải loại bỏ.
Một số enzyme dưới đây là lựa chọn phổ biến cho việc tạo khuôn bằng enzyme cắt giới hạn: