Năm 1975, César Milstein và Georges Köhler đã công bố một phương pháp tạo ra vô số kháng thể giống hệt nhau. Bằng cách dung hợp tế bào B miễn dịch với tế bào u tủy, họ đã tạo ra các hybridoma – những dòng tế bào bất tử có thể tiết ra một loại kháng thể đặc hiệu vô thời hạn. Họ khiêm tốn kết luận rằng những kháng thể đơn dòng (mAb) này “có thể có giá trị cho ứng dụng y tế và công nghiệp“.
Tất nhiên, nhận định này hóa ra còn quá khiêm tốn. Năm 2025, các biên tập viên của tạp chí Nature đã viết rằng phát minh này “có một trong những tác động lớn nhất đến khoa học và chăm sóc sức khỏe trong thời kỳ hiện đại“. Ngày nay, thị trường kháng thể đơn dòng đã đạt 250 tỷ đô la và vẫn tiếp tục tăng, với hàng chục triệu bệnh nhân đã được điều trị. Và tác động của nó vượt xa y học. Như Nature đã nhận xét, mAb hiện nay là “cỗ máy lao động chính trong các phòng thí nghiệm nghiên cứu“. Công nghệ cần thiết để sản xuất, tinh sạch và nghiên cứu chúng cũng vậy.
Điều đó đã diễn ra như thế nào? Nhiều người đã nhận ra tiềm năng của mAb từ sớm, nhưng con đường phía trước “đầy cạm bẫy và khó khăn“, như Milstein đã nói trong bài giảng Nobel năm 1984. Một trong những thách thức không nhỏ là xây dựng một hệ thống kiến thức về cấu trúc và tương tác phân tử, cơ chế bệnh học, và các mục tiêu thuốc mà mAb có thể tác động. Dù đáng chú ý đến thế nào, phát minh của Milstein và Köhler cũng chỉ là một đỉnh núi trong một dãy núi trải dài bao gồm sinh học cấu trúc, nghiên cứu protein, miễn dịch học, kỹ thuật cơ khí, thiết kế protein tính toán và sinh học phân tử – cùng nhiều lĩnh vực khác.
Cũng giống như không có hai chuyến thám hiểm leo núi nào giống hệt nhau, mỗi bước đột phá khoa học đều có một con đường riêng. Điểm chung của tất cả là sự phụ thuộc lẫn nhau: những cột mốc, một khi đã đạt được, sẽ trở thành những bậc thang. Bài báo năm 1975 của Milstein và Köhler vừa là đỉnh cao của – vừa là điểm khởi đầu cho – nhiều thập kỷ tích lũy những hiểu biết sâu sắc và tiến bộ công nghệ. Tại đây, chúng ta sẽ nhìn lại một số điểm sáng.

Sự trỗi dậy của sinh học phân tử và khoa học protein
Câu chuyện của chúng ta bắt đầu sau một cuộc cách mạng khoa học đặt các phân tử sinh học vào vị trí trung tâm. Giữa năm 1940 và 1965, một loạt các khám phá đã đặt nền móng cho sinh học phân tử. Các nhà khoa học đã xác nhận DNA mang thông tin di truyền và phát hiện ra mối quan hệ trực tiếp giữa gen và protein. Những hiểu biết này đã đạt đến đỉnh cao với việc mô tả học thuyết trung tâm: dòng thông tin di truyền từ DNA đến RNA và đến protein.
Những bước tiến vượt bậc về mặt lý thuyết này được thúc đẩy bởi đổi mới công nghệ. Kỹ thuật nhiễu xạ tia X đã tiết lộ cấu trúc ba chiều của phân tử; siêu ly tâm giúp phân tách protein theo kích thước và tỷ trọng tốt hơn; điện di phân biệt protein và axit nucleic theo kích thước và điện tích.
Làn sóng tiến bộ tiếp theo – tạo ra phân tử DNA tái tổ hợp đầu tiên vào năm 1972, mAb có nguồn gốc từ hybridoma của Milstein và Köhler vào năm 1975, và insulin người tái tổ hợp vào năm 1978 – đã mở ra nhiều con đường hơn nữa. Nhưng hành trình leo lên trở nên dốc hơn. Insulin tái tổ hợp vẫn phải được tách khỏi các tạp chất từ tế bào. mAb từ hybridoma của chuột nhắt hoặc chuột cống rất khó sản xuất và có nguy cơ gây tác dụng phụ nghiêm trọng trên người. Tương tự, việc nghiên cứu enzyme, thụ thể và các protein khác phụ thuộc vào việc phân lập chúng từ hỗn hợp phức tạp. Công nghệ tinh sạch protein có thể giúp giải quyết những vấn đề này, nhưng những hạn chế của nó đã làm chậm tiến độ.
Các chiến lược tinh sạch ban đầu như kết tủa bằng dung môi hoặc muối và siêu ly tâm, nhiều phương pháp vẫn được sử dụng cho đến ngày nay, đóng vai trò then chốt. Tuy nhiên, chúng có thể chậm, và hiệu suất cũng như độ tinh khiết có thể thay đổi đáng kể giữa các lần chạy. Sắc ký lỏng có thể giúp ích ở đây. Trong kỹ thuật này, các chất phân tích trong pha động (như dịch nuôi cấy tế bào) di chuyển qua pha tĩnh bao gồm các hạt hoặc hạt nhỏ được đóng gói. Các hạt này sẽ tách phân tử quan tâm khỏi phần còn lại của dịch nổi khi nó đi qua. Quá trình này có thể xảy ra nhờ cơ chế loại trừ kích thước (nơi các phân tử quá lớn không thể đi qua sẽ bị giữ lại trong các hạt), nhờ ái lực (nơi các phân tử liên kết với phối tử gắn trên các hạt), hoặc nhờ các cơ chế khác. Dù cơ chế nào, kết quả vẫn giống nhau: tách protein quan tâm ra khỏi hỗn hợp. Các hệ thống ban đầu dựa vào trọng lực để kéo pha động đi qua, dẫn đến quá trình phân tách chậm, khó tái lập và thường có độ phân giải thấp – một nền tảng khó khăn cho các nhà nghiên cứu đang cố gắng giữ vững các phân tử sinh học còn nguyên vẹn.
Sắc ký lỏng hiệu năng cao (HPLC), nổi lên vào những năm 1960 và 1970, là một phương tiện để phân tách phân tử nhanh hơn và chính xác hơn. Bằng cách kết hợp bơm áp suất cao với kích thước hạt nhựa nhỏ, HPLC cung cấp khả năng phân tách nhanh hơn, được kiểm soát tốt hơn với độ phân giải được cải thiện đáng kể. Nhưng áp suất cao (hàng chục đến hàng trăm bar) và việc sử dụng dung môi hữu cơ có thể làm biến tính các phân tử sinh học nhạy cảm. Đối với các nhà nghiên cứu đang leo lên mục tiêu phân lập các protein còn nguyên vẹn, có chức năng – như những protein cho các liệu pháp mAb trong tương lai – cần một con đường nhẹ nhàng hơn.
Phân tách cho các phân tử nhạy cảm
Một giải pháp thay thế tương thích sinh học cho HPLC là mục tiêu của các nhà khoa học tại Pharmacia Fine Chemicals (nay là Cytiva) ở Uppsala, Thụy Điển, bắt đầu từ năm 1975. Họ tìm kiếm một hệ thống vừa giữ được độ phân giải cao của HPLC vừa bảo vệ các phân tử sinh học mỏng manh.
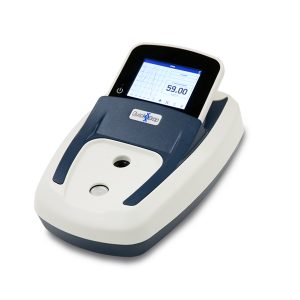
Sau bảy năm nghiên cứu chuyên sâu, thử nghiệm và phát hành từng mô-đun, hệ thống FPLC hoàn chỉnh đầu tiên đã ra mắt (Hình 1). Ban đầu được đặt tên là sắc ký lỏng hiệu năng nhanh (fast performance liquid chromatography – FPLC) để phân biệt với HPLC, đây là hệ thống tích hợp đầu tiên trên thế giới được thiết kế đặc biệt cho sắc ký điều chế. Trong khi HPLC tập trung vào định tính phân tích, FPLC được tạo ra rõ ràng cho mục đích tinh sạch sinh học.
FPLC cho phép phân tách các đại phân tử ở áp suất nhẹ (<5 bar). Các cột được nhồi với hạt agarose liên kết ngang có đường kính hạt lớn hơn, cho phép tốc độ dòng cao hơn so với phân tách dựa trên trọng lực, ở áp suất đủ thấp để giữ cho mẫu được nguyên vẹn.
Đạt độ cao mới với FPLC
Khi các nhà khoa học đã có công cụ mới này trong hành trang, tiến độ nhanh chóng được đẩy nhanh. Ngay từ năm 1985, các ấn phẩm mang tính bước ngoặt đã sử dụng FPLC để tinh sạch protein. Ví dụ, Bruce Beutler đã mô tả trong bài giảng Nobel của mình về khó khăn trong việc bảo toàn cấu trúc bậc một của cachectin chuột được tinh sạch từ môi trường điều hòa đại thực bào. Ông đã sử dụng hệ thống FPLC của Pharmacia để phát triển phương pháp cuối cùng mang lại trình tự axit amin chính xác. Trình tự này tiết lộ rằng cachectin là ortholog ở chuột của yếu tố hoại tử khối u (TNF) ở người, một phát hiện đóng vai trò nền tảng trong công trình mà Beutler đã giành giải Nobel năm 2011.
Hệ thống FPLC nhanh chóng trở thành một công cụ linh hoạt trên nhiều lĩnh vực, tinh sạch đủ mọi thứ từ yếu tố tăng trưởng tế bào B và mAb đến các phân tử truyền tín hiệu ở tế bào thực vật. Nó hỗ trợ các công trình then chốt của các nhà khoa học như Steven McKnight, Franz Ulrich Hartl và những người khác, những người đã dựa vào FPLC để phân lập protein liên kết nhân, enzyme liên quan đến quá trình gấp cuộn và nucleotide. FPLC hoạt động như một sợi dây an toàn vững chắc cho các dự án này, hỗ trợ sự tiến bộ ổn định lên đỉnh trên nhiều địa hình khoa học đa dạng.

Một cuộc thám hiểm táo bạo: chinh phục đỉnh Ribosome
Trong suốt giai đoạn này, một cuộc săn lùng toàn cầu đầy tham vọng khác cũng đang diễn ra: giải mã cấu trúc ribosome ở độ phân giải nguyên tử. Ribosome – ở vi khuẩn, là một phức hợp RNA-protein khổng lồ khoảng 2,5 triệu Da – đóng vai trò thiết yếu trong việc dịch mã thông tin di truyền. Nó cũng là một mục tiêu thuốc quan trọng. Hơn một nửa số kháng sinh lâm sàng liên kết với ribosome, và việc giải mã cấu trúc nguyên tử sẽ cho phép thiết kế các loại kháng sinh mới.
Tuy nhiên, việc kết tinh ribosome đặt ra những thách thức phi thường. Như một trong các nhà nghiên cứu sau này đã nói, “ý tưởng kết tinh ribosome là hoàn toàn điên rồ”. Nhưng vẫn có những tiến triển. Ada Yonath tại Viện Khoa học Weizmann ở Israel đã đạt được bước đệm vào năm 1980, giải quyết vấn đề độ phân giải thấp ở ribosome đã tinh sạch. Các nhóm khác, bao gồm Thomas Steitz tại Yale và Venkatraman Ramakrishnan tại Phòng thí nghiệm Sinh học Phân tử MRC ở Cambridge, đã leo cao hơn nữa, thu được tinh thể nhiễu xạ ở mức 7–9 Å vào cuối những năm 1990.
Như Ada Yonath đã nói với Ủy ban Nobel năm 2009: “Những gì chúng tôi cảm thấy là chúng tôi đang leo lên những ngọn núi để lên đến đỉnh cao – và những ngọn núi này giống như đỉnh Everest, lớn nhất và khó leo nhất – chỉ để nhận ra rằng có một ngọn núi khác đang chờ phía sau để leo tiếp”.
Tinh sạch không phải là thách thức lớn nhất trong cuộc thám hiểm này, mà chỉ là một trong những trạm dừng. Ribosome rất mỏng manh và dễ bị phân rã dưới áp lực cắt hoặc điều kiện muối không phù hợp. Kỹ thuật tinh thể học đòi hỏi các tiểu phần ribosome có độ tinh khiết cao, đồng nhất và ở nồng độ cao – không có nuclease và protease. Công cụ được lựa chọn cho công việc này là FPLC sử dụng tương tác kỵ nước.
Năm 2000, sau nhiều thập kỷ tiến triển từng bước, ba nhóm đã lên đến đỉnh. Nhóm của Steitz giải mã tiểu phần 50S, nhóm của Yonath độc lập giải mã tiểu phần 50S, và phòng thí nghiệm của Ramakrishnan giải mã tiểu phần 30S. Nỗ lực này là một kỳ công về công nghệ, mang về cho Ramakrishnan, Steitz và Yonath giải Nobel Hóa học năm 2009.
Vào thời điểm đó, FPLC đã khẳng định vị trí của mình trong số các công nghệ then chốt. Khi các nhà khoa học tiếp tục tìm ra những cách thông minh để tận dụng công nghệ này, hệ thống FPLC của Pharmacia cũng đang phát triển để làm cho việc tinh sạch trở nên dễ tiếp cận hơn với nhiều người dùng hơn.
Những con đường mới và những đỉnh cao vươn lên: các cuộc thám hiểm vào vùng đất khám phá
Khi một đỉnh cao đã đạt được, những đỉnh cao mới lại hiện ra. Khi sinh học cấu trúc mở rộng, FPLC vẫn giữ vai trò trung tâm. Roderick MacKinnon đã sử dụng FPLC để tinh sạch các protein nối kết (junctional proteins) cho nghiên cứu tinh thể học, công trình đã mang về cho ông giải Nobel Hóa học năm 2003 nhờ làm sáng tỏ cấu trúc và chức năng của kênh ion. Sự hiểu biết này đã đặt nền móng cho việc hiểu và điều trị các bệnh liên quan đến rối loạn chức năng kênh ion, như rối loạn nhịp tim, rối loạn thần kinh và rối loạn tự miễn. Công nghệ FPLC đã hỗ trợ tinh sạch cho các nghiên cứu về yếu tố phiên mã, sinh học ty thể, virus viêm gan C và các cơ chế enzyme độc đáo.
Tinh sạch protein cho các ứng dụng hạ nguồn trở nên quan trọng không kém việc tinh sạch chúng cho phân tích cấu trúc. Frances Arnold đã tiên phong trong lĩnh vực tiến hóa định hướng từ những năm 1990 và 2000, tạo ra các enzyme với chức năng được tăng cường hoặc hoàn toàn mới. Công trình đoạt giải Nobel của bà là nền tảng trong khoa học đời sống cũng như trong phát triển và sản xuất thuốc. Ví dụ, trong sản xuất dược phẩm, tiến hóa định hướng đã được sử dụng để tối ưu hóa các sản phẩm thuốc và quy trình sản xuất nhằm cải thiện hiệu quả và độ an toàn. Alex Winter, người chia sẻ giải Nobel Hóa học với Arnold vào năm 2018, đã sử dụng tiến hóa định hướng trên protein để phát triển các liệu pháp sinh học. Ngày nay, tiến hóa định hướng thường xuyên được sử dụng để thay đổi các dược phẩm sinh học nhằm tăng độ hòa tan, khả năng tinh sạch, độ ổn định và giảm tính sinh miễn dịch. Loại thuốc đầu tiên được đưa ra thị trường phát triển bằng phương pháp này là adalimumab, được phê duyệt năm 2002 để điều trị viêm khớp dạng thấp và các bệnh tự miễn khác.
Để hiện thực hóa tiềm năng của các enzyme và protein được thiết kế, cũng như bất kỳ cuộc thám hiểm nào, cần có công cụ phù hợp. Khả năng mở rộng quy mô là chìa khóa, và điều đó đòi hỏi khả năng tinh sạch các phân tử đích một cách dễ dự đoán, thông lượng cao, sử dụng phương pháp không làm gián đoạn chức năng của chúng. Một lần nữa, FPLC là phương pháp được nhiều nhà khoa học lựa chọn.
Lúc này, công nghệ FPLC đã trở nên tinh vi hơn. Quá trình tinh sạch có thể được tự động hóa nhờ các hệ thống như hệ thống sắc ký SMART của Pharmacia, ra mắt năm 1990, và phiên bản kế tiếp, hệ thống ÄKTAexplorer, ra mắt năm 1996. Tự động hóa và tiêu chuẩn hóa phần mềm điều khiển càng mở rộng khả năng của các nhà khoa học, cho phép họ tận dụng thông lượng cao hơn, quy trình đơn giản hóa và kết quả có tính tái lập cao hơn.
Chinh phục điều không tưởng: nhóm CRISPR tiến công đỉnh cao
Năm 2012, thế giới biết đến CRISPR-Cas9, một hệ thống miễn dịch của vi khuẩn được tái sử dụng thành công cụ chỉnh sửa gen, và sinh học đã không còn như trước. Nhưng đây là một hành trình leo dốc đòi hỏi độ chính xác kỹ thuật cao. Ý tưởng cơ bản rất táo bạo: liệu các nhà nghiên cứu có thể tạo ra một hệ thống trong đó protein vi khuẩn (Cas9), được dẫn dắt bởi một RNA nhỏ, có thể cắt DNA tại một vị trí mong muốn? Nếu được, nó sẽ cung cấp một cách dễ dàng để chỉnh sửa bộ gen.
Jennifer Doudna và Emmanuelle Charpentier đã dẫn dắt cuộc chinh phục này. Những công cụ họ sử dụng dọc đường không hào nhoáng, nhưng rất đáng tin cậy. Công việc bao gồm biểu hiện quá mức Cas9 trong E. coli và tinh sạch nó bằng quy trình sắc ký nhiều bước. Các thành phần RNA được tổng hợp bằng phiên mã in vitro và tinh sạch (thường bằng sắc ký). Khi họ trộn Cas9 đã tinh sạch với crRNA, tracrRNA và DNA đích, họ đã quan sát thấy một vết cắt chính xác tại vị trí dự đoán.
Khả năng dễ dàng cắt DNA tại các vị trí đã chọn, một khi được chứng minh, đã tạo ra một hiệu ứng dây chuyền. Như Doudna sau này đã nói, “Chúng tôi đã có linh cảm trong những ngày đầu tiên đó, trong công trình của tôi với Emmanuelle, rằng… chúng tôi đã chạm vào một điều gì đó lớn lao, nhưng tôi nghĩ chúng tôi đã không biết nó lớn đến mức nào”. Trong vòng vài tháng, một số nhóm đã chỉ ra rằng CRISPR-Cas9 có thể chỉnh sửa gen bên trong tế bào động vật có vú sống. Sự đơn giản của hệ thống đã giúp nhiều phòng thí nghiệm có thể tiếp cận, dẫn đến vô số tiến bộ: tạo mô hình bệnh, thiết kế cây trồng, phát triển các liệu pháp mới (liệu pháp gen dựa trên CRISPR đã cho thấy nhiều hứa hẹn trong việc điều trị các bệnh di truyền trong các thử nghiệm lâm sàng). Thật khó để nói quá tác động của CRISPR. Nhưng không gì trong số này có thể xảy ra nếu Charpentier và Doudna không chứng minh được đầu tiên rằng phản ứng sinh hóa hoạt động. Và bằng chứng đó dựa trên những công cụ của nghề: không chỉ FPLC, mà còn cả bộ kit nhân dòng gen, vector biểu hiện, và các cột tinh sạch cùng quy trình để thu được Cas9 có hoạt tính.
Mở rộng quy mô khoa học thành y học
Ở những nơi khác, các nhà leo núi đang tiến hành nghiên cứu miễn dịch học, mở đường cho các liệu pháp miễn dịch hiện đại. Công trình này cũng phụ thuộc vào việc phân lập các thụ thể, phân tử tín hiệu và kháng thể. Các nền tảng tinh sạch ngày càng trở nên quan trọng trong sản xuất kháng thể, hỗ trợ cho mAb điều trị, kháng thể hai đặc hiệu (bispecifics) và kháng thể liên hợp thuốc (ADC).
Nhưng việc lên đến đỉnh chỉ là một nửa hành trình; việc đưa các khám phá trở về an toàn để đến tay bệnh nhân cũng đòi hỏi không kém. Các hệ thống tinh sạch tỏ ra không thể thiếu trong sản xuất sinh học cũng như trong phòng thí nghiệm nghiên cứu. Các nền tảng FPLC đã trở thành công cụ nền tảng trong xử lý sinh học công nghiệp, cho phép các quy trình vận hành từ quy mô phòng thí nghiệm đến quy mô sản xuất. Khả năng mở rộng quy mô của các công nghệ hỗ trợ, như các hệ thống ÄKTA™ ngày nay phổ biến trong các phòng thí nghiệm và khu sản xuất, đã giúp chuyển giao các quy trình một cách liền mạch vào môi trường sản xuất. Các nền tảng như vậy đã hỗ trợ tinh sạch mAb, kháng thể hai đặc hiệu, protein tái tổ hợp, yếu tố tăng trưởng và các dược phẩm sinh học khác. Các hệ thống FPLC đầu tiên đã đóng góp vào việc phát triển rituximab, mAb đầu tiên được phê duyệt cho bệnh ung thư và là liệu pháp nhắm mục tiêu tế bào B đầu tiên cho bệnh ung thư.

Tinh sạch axit nucleic cũng đã chuyển đổi nhanh chóng. Trong quá trình phát triển vắc-xin mRNA vào những năm 2010, các nhóm do Katalin Karikó và Drew Weissman dẫn đầu đã sử dụng hệ thống ÄKTA™ để sản xuất mRNA cho các nghiên cứu tiền lâm sàng và về hạt nano lipid. Trong đại dịch COVID‑19, việc sản xuất mRNA tinh sạch trên toàn cầu đòi hỏi sự mở rộng quy mô chưa từng có – một nỗ lực được thực hiện thành công, một phần nhờ vào các hệ thống sắc ký được thiết kế để leo dốc êm ái từ quy mô bàn thí nghiệm đến sản xuất lớn.
Nhìn về những đường gờ núi phía trước
Trong kỷ nguyên sinh học tổng hợp và tính toán – nơi học máy thiết kế các enzyme mới và trí tuệ nhân tạo dự đoán cấu trúc protein – các hệ thống ÄKTA™ tiếp tục đóng vai trò là cầu nối giữa thiết kế trong máy tính và xác thực trong thế giới thực. Chúng giúp đảm bảo rằng các cấu trúc tổng hợp không chỉ phù hợp với dự đoán mà còn hoạt động như mong đợi.
Người đoạt giải Nobel David Baker đã sử dụng hệ thống ÄKTA™ để tinh sạch các protein được thiết kế bằng thuật toán. Tương tự, các nhà nghiên cứu tại Google đã dựa vào hệ thống ÄKTA pure™ để xác nhận hoạt tính của các protein được tạo ra bằng hệ thống học máy AlphaProteo của họ. Thực vậy, các công cụ thiết kế protein de novo như AlphaFold và RFdiffusion đã không thể có được nếu không có FPLC. Các mô hình như vậy được đào tạo trên dữ liệu cấu trúc protein được tạo ra bởi cộng đồng nghiên cứu trong nhiều thập kỷ qua. Tính đến tháng 2 năm 2026, Ngân hàng Dữ liệu Protein (Protein Data Bank) chứa gần 250.000 cấu trúc protein được xác định bằng thực nghiệm. Hầu hết trong số này đã được tinh sạch bằng FPLC.
Thật khó để nói, khi đứng trên đỉnh núi, rằng một đoạn đường nào đó quan trọng hơn bất kỳ đoạn đường nào khác. Trong bức tranh toàn cảnh về những đỉnh cao khoa học này, mỗi bước đi đều xuất phát từ nhiều thập kỷ hiểu biết sâu sắc, sự kiên trì và những đổi mới đã có từ trước. Tuy nhiên, khi các nhà khoa học sẵn sàng tiến lên, những công cụ tinh sạch trong tay họ thường quyết định họ có thể leo xa và an toàn đến mức nào. Từ những hybridoma đầu tiên đến các protein do AI thiết kế ngày nay, các hệ thống như FPLC và hệ thống sắc ký ÄKTA™ đã giúp biến những hiểu biết sâu sắc thành đột phá, và đột phá thành liệu pháp. Khi những thách thức mới xuất hiện phía chân trời, những công nghệ này sẽ tiếp tục hỗ trợ vững chắc cho hành trình chinh phục.