Giới thiệu
Exosome có nguồn gốc từ tế bào gốc trung mô (MSC) đang ngày càng được chú ý như những công cụ mạnh mẽ trong y học tái tạo, phân phối thuốc và điều hòa miễn dịch. Khả năng mang theo các phân tử có hoạt tính sinh học khiến chúng trở thành các ứng viên điều trị đầy tiềm năng; tuy nhiên, việc mở rộng quy mô sản xuất trong khi vẫn duy trì hiệu suất và chất lượng cao vẫn là một thách thức quan trọng, ảnh hưởng đến hiệu quả chi phí và khả năng tiếp cận của bệnh nhân.
Nền tảng bioreactor giá thể cố định có cấu trúc (structured fixed-bed bioreactor) scale-X của Univercells Technologies cung cấp một môi trường được kiểm soát, lực cắt thấp cho nuôi cấy tế bào bám dính mật độ cao trong môi trường không huyết thanh (SFM), cho phép tăng cường và mở rộng quy mô sản xuất exosome. Nền tảng scale-X (diện tích tăng trưởng 0,5–600 m²) cho phép chuyển giao quy trình liền mạch từ giai đoạn phát triển sang quy mô thương mại.
Các bioreactor này được cấu tạo từ hai lớp polymer không dệt ưa nước để giữ và hỗ trợ tăng sinh tế bào, cùng với một lớp đệm kỵ nước giúp phân phối môi trường nuôi cấy đồng đều (Hình 1). Danh mục sản phẩm cung cấp dải quy mô có khả năng mở rộng hoàn chỉnh, từ scale-X nexo (0,5 m²), scale-X hydro (2,4 m²), scale-X carbo (10–30 m²) đến scale-X nitro (200–600 m²).
Các trường hợp thành công với scale-X
Các bioreactor giá thể cố định scale-X đã chứng minh khả năng sản xuất cao các túi ngoại bào (EV), bao gồm exosome, ở nhiều quy mô khác nhau. Trong nghiên cứu này, chúng tôi trình bày 3 case study sử dụng các loại tế bào MSC khác nhau để sản xuất EV: RoosterBio và Asfreya sử dụng bioreactor scale-X hydro (2,4 m²) và Orbsen Therapeutics sử dụng bioreactor scale-X carbo (10 m²) tích hợp hệ thống lọc dòng chảy tiếp tuyến (TFF).
1. Tăng sinh hMSC và sản xuất túi ngoại bào trong scale-X hydro

RoosterBio đã thiết lập quy trình sản xuất EV trong hệ 2D sử dụng môi trường không huyết thanh được phát triển cho sản xuất EV. Để tăng năng suất ở quy mô lớn hơn và trong môi trường được kiểm soát tốt hơn, họ đã phát triển quy trình sử dụng scale-X hydro. Tế bào gốc trung mô người (hMSC) được tăng sinh trong các bình nuôi 2D. Sau khi đạt mật độ tế bào mong muốn trong scale-X hydro, môi trường nuôi cấy đã điều hòa chứa EV được thu hoạch trong vòng 7 ngày và tiếp tục được phân tích ở các bước tiếp theo.
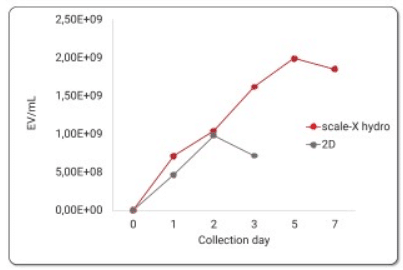
Sản xuất EV trong scale-X hydro
Cho phép kéo dài giai đoạn sản xuất từ ngày 3 đến ngày 7 của quy trình;
Cung cấp nồng độ EV cao hơn 2,5 lần so với đối chứng 2D vào ngày thứ 3 của quy trình (Hình 2);
- Chuyển giao thành công các nuôi cấy hMSC sản xuất EV từ hệ thống 2D.
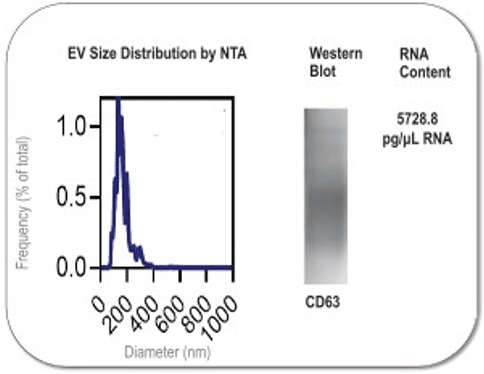
Đặc tính EV
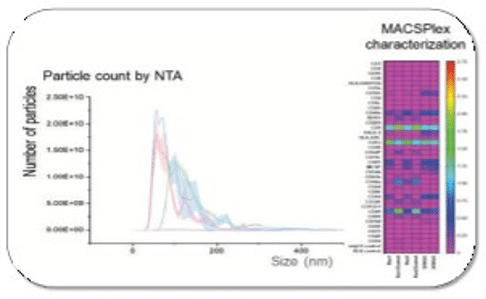
- EV đáp ứng các đặc tính đã được mô tả ở tế bào MSC người, với kích thước trong khoảng 50–400 nm (Hình 3);
- Tất cả các lần chạy đều biểu hiện protein xuyên màng tetraspanin (CD63 – gen mã hóa ở người);
- Tất cả các lần chạy đều có chứa microRNA, vốn được biết là một trong những phân tử được vận chuyển bởi EV.
2. Đạt được năng suất sản xuất túi ngoại bào vượt trội bằng bioreactor scale-X hydro

Để nâng cao năng suất và kiểm soát quy trình, đồng thời khắc phục các hạn chế về khả năng mở rộng của hệ nuôi cấy 2D, Asfreya đã chuyển quy trình sản xuất EV sang bioreactor scale-X hydro. EV được sản xuất từ tế bào WJ-MSC của Asfreya được nuôi trong môi trường MesenCult-ACF Plus bổ sung glutamine và G418. Trong quá trình sản xuất với scale-X hydro, bioreactor được vận hành với pha thu hoạch EV kéo dài 48 giờ. Việc đánh giá chất lượng EV được thực hiện bằng phân tích Nanosight và ExoScreen. Là đối chứng, EV được sản xuất bằng quy trình nuôi cấy đĩa 2D đã được thiết lập của Asfreya.
Sản xuất EV trong scale-X hydro
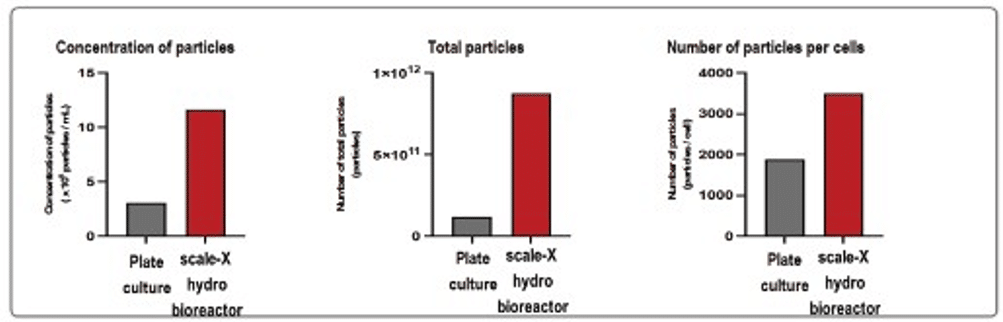
Hệ thống scale-X hydro cho thấy năng suất tăng 1,5 lần so với quy trình 2D (Hình 4).
Đặc tính EV
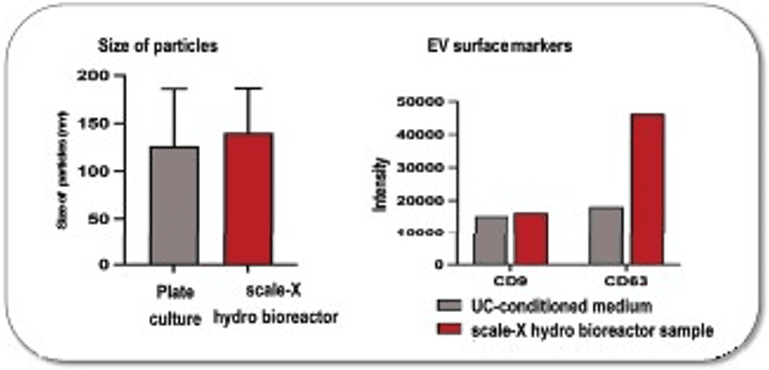
So với nuôi cấy đĩa 2D, EV thu được từ bioreactor scale-X hydro đáp ứng các tiêu chí chất lượng quan trọng, dựa trên phân tích kích thước hạt và các marker bề mặt CD9/CD63 (Hình 5).
3. Quy trình sản xuất túi ngoại bào theo chế độ perfusion trong scale-X carbo

Trường hợp sản xuất EV cuối cùng không chỉ nhằm mở rộng quy mô quy trình từ bình nuôi trực tiếp lên carbo 10 m² mà còn tích hợp lọc dòng chảy tiếp tuyến (TFF) để thực hiện quy trình perfusion liên tục và cô đặc. Orbsen đã chuyển quy trình sản xuất EV sang hệ thống scale-X carbo, tích hợp bộ điều khiển và bioreactor giá thể cố định cùng với quy trình sinh học có khả năng perfusion với mô-đun TFF in-line, giúp thu hoạch và cô đặc EV liên tục. Tế bào gốc trung mô từ dây rốn (UC-MSC) được nuôi cấy trong bioreactor scale-X carbo 10 m² trong 9 ngày trước khi bắt đầu sản xuất EV dưới điều kiện perfusion.
Sản xuất EV trong scale-X carbo
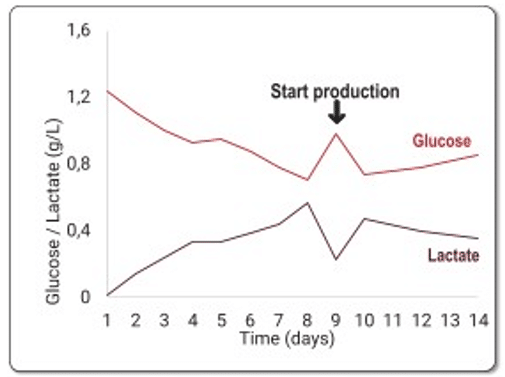
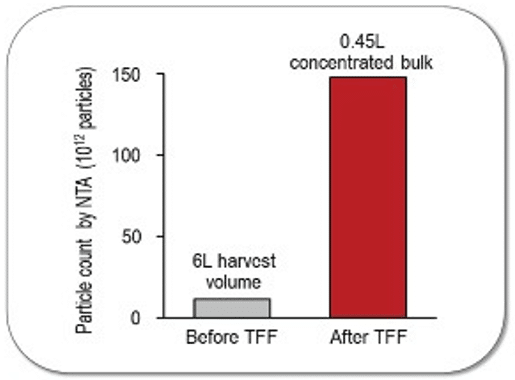
Trong quá trình perfusion, glucose và lactate được theo dõi hằng ngày, và hệ thống duy trì được mức ổn định (Hình 6). Nhờ sử dụng TFF tích hợp, đạt được mức cô đặc EV gấp 13 lần (Hình 7). Hệ thống cho thấy khả năng giảm thời gian xử lý và thể tích thu hoạch tổng, từ đó đơn giản hóa các bước downstream.
Đặc tính EV
Việc đặc trưng EV trong khoảng kích thước 100–400 nm đáp ứng các tiêu chí chất lượng quan trọng yêu cầu cho sản phẩm này (Hình 8).
Kết luận và Các điểm nổi bật
Trong nghiên cứu đa trường hợp, các bioreactor scale-X hydro và scale-X carbo đã chứng minh thành công khả năng mở rộng quy trình nuôi cấy hMSC sản xuất EV trong điều kiện bám dính và không huyết thanh, với các kết quả:
- Tăng hiệu giá gấp 2 lần trên mỗi tế bào và gấp 3 lần trên mỗi mL so với hệ thống 2D;
- Kéo dài thời gian thu hoạch EV (+2 ngày);
- Tích hợp hiệu quả perfusion và cô đặc bằng TFF, tạo ra sản phẩm cuối có độ cô đặc cao hơn và sạch hơn;
- Các đặc tính chất lượng exosome ổn định, phù hợp với tiêu chuẩn công nghiệp.