Không chắc nên sử dụng ELISA hay ELISpot? Hướng dẫn này phân tích sự khác biệt để giúp bạn lựa chọn xét nghiệm phù hợp nhất cho dự án của mình.
Giới thiệu
Trong nghiên cứu y sinh, việc đo lường protein như cytokine, kháng thể hoặc yếu tố tăng trưởng là rất quan trọng để hiểu đáp ứng miễn dịch, tiến triển bệnh và hiệu quả điều trị. Trong số các công cụ cho mục đích này có ELISA (Enzyme-Linked Immunosorbent Assay) và ELISpot (Enzyme-Linked ImmunoSpot).
Mặc dù cả hai kỹ thuật đều dựa trên phát hiện bằng kháng thể và khuếch đại tín hiệu nhờ enzyme, chúng phục vụ các mục tiêu thí nghiệm khác nhau. ELISA định lượng lượng protein cụ thể trong mẫu, trong khi ELISpot định lượng các tế bào riêng lẻ đang sản xuất protein đó.
Vậy làm thế nào để quyết định xét nghiệm nào phù hợp nhất cho nghiên cứu của bạn? Trong bài viết này, chúng tôi sẽ phân tích các nguyên lý chính, ứng dụng và sự khác biệt giữa ELISA và ELISpot để giúp bạn chọn đúng công cụ cho thí nghiệm tiếp theo.
ELISA là gì?
ELISA (Enzyme-Linked Immunosorbent Assay) là một trong những xét nghiệm miễn dịch được sử dụng rộng rãi nhất để phát hiện và định lượng các protein hòa tan như cytokine, kháng thể và hormone trong các dịch sinh học như huyết thanh, huyết tương hoặc dịch nổi nuôi cấy tế bào. Phương pháp này hoạt động bằng cách bắt giữ chất phân tích mục tiêu bằng các kháng thể đặc hiệu và tạo ra tín hiệu có thể đo được, thường là tín hiệu màu, tương quan với nồng độ của chất phân tích.
Nổi tiếng với độ ổn định, khả năng mở rộng và đầu ra định lượng, ELISA là phương pháp phổ biến trong chẩn đoán, xác nhận biomarker và xét nghiệm thường quy trong phòng thí nghiệm. Mặc dù không cung cấp thông tin về nguồn tế bào của chất phân tích, ELISA vượt trội trong việc cung cấp dữ liệu nồng độ chính xác và có khả năng lặp lại trên số lượng lớn mẫu.
Các loại ELISA
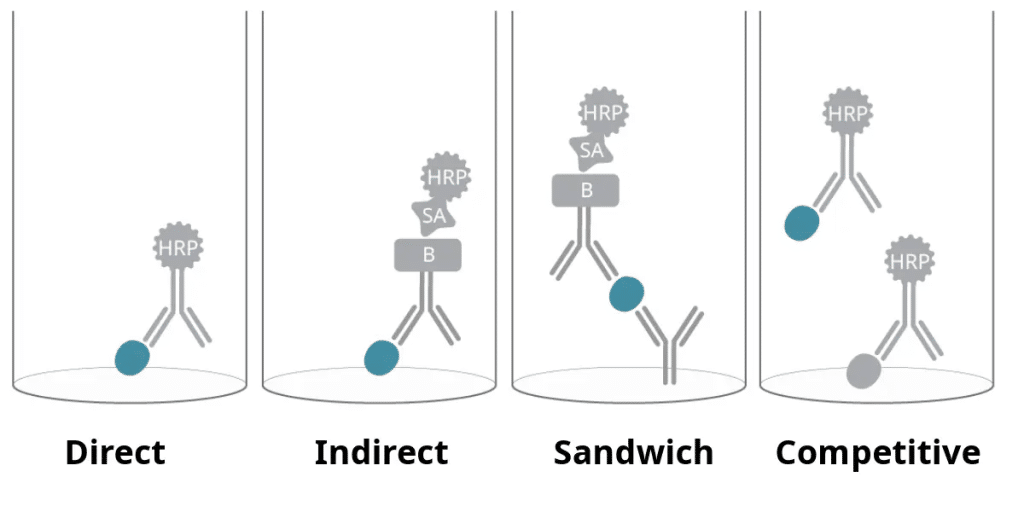
Bốn loại ELISA chính là ELISA trực tiếp, gián tiếp, sandwich và cạnh tranh.
- ELISA trực tiếp sử dụng kháng thể sơ cấp được gắn enzyme. Định dạng này có quy trình đơn giản và nhanh chóng nhưng thường có độ nhạy thấp hơn do khả năng khuếch đại tín hiệu hạn chế.
- ELISA gián tiếp tăng độ nhạy bằng cách sử dụng hệ phát hiện hai bước bao gồm kháng thể sơ cấp và sau đó là kháng thể thứ cấp gắn enzyme. Cách thiết lập này cho phép khuếch đại tín hiệu nhưng có thể gây phản ứng chéo, đặc biệt khi sử dụng kháng thể thứ cấp được tạo ra từ cùng loài với kháng thể sơ cấp.
- ELISA sandwich có độ đặc hiệu cao và lý tưởng để phát hiện chất phân tích trong các mẫu phức tạp. Phương pháp này dựa trên hai kháng thể: kháng thể bắt giữ được phủ trên đáy giếng để cố định kháng nguyên mục tiêu và kháng thể phát hiện gắn vào epitope khác trên cùng kháng nguyên. Mặc dù yêu cầu cặp kháng thể phù hợp, độ đặc hiệu và độ nhạy cao khiến đây là phương pháp được ưu tiên, đặc biệt để định lượng các chất có nồng độ thấp trong các nền mẫu phức tạp.
- ELISA cạnh tranh phù hợp nhất cho các phân tử nhỏ hoặc kháng nguyên có ít epitope. Trong định dạng này, kháng nguyên trong mẫu cạnh tranh với kháng nguyên được đánh dấu để gắn vào kháng thể. Phương pháp này có độ nhạy cao nhưng thiết lập phức tạp hơn và tín hiệu đọc ngược (tín hiệu giảm khi nồng độ kháng nguyên tăng).
Khi sử dụng ELISA để phát hiện immunoglobulin, thiết kế xét nghiệm cần được điều chỉnh phù hợp với câu hỏi nghiên cứu cụ thể. Tìm hiểu thêm.
Tóm lại, mỗi định dạng ELISA đều có ưu điểm và hạn chế riêng. Việc lựa chọn loại phù hợp phụ thuộc vào nhu cầu thí nghiệm và các thuốc thử sẵn có.
Cơ chế hoạt động
Trong ELISA sandwich, một đĩa có khả năng gắn kết cao được phủ kháng thể bắt giữ đặc hiệu với protein mục tiêu. Sau bước blocking để ngăn gắn kết không đặc hiệu, mẫu và chuẩn được thêm vào, cho phép protein mục tiêu gắn vào kháng thể bắt giữ. Sau đó, kháng thể phát hiện được gắn biotin sẽ được thêm vào và gắn vào epitope khác trên cùng protein. Tiếp theo là phức hợp streptavidin–enzyme. Khi thêm cơ chất tạo màu, enzyme sẽ tạo ra tín hiệu nhìn thấy được, tỷ lệ thuận với lượng protein có trong mẫu. Tín hiệu được đo bằng máy đọc đĩa và định lượng bằng cách so sánh với đường chuẩn.
Kết quả ELISA
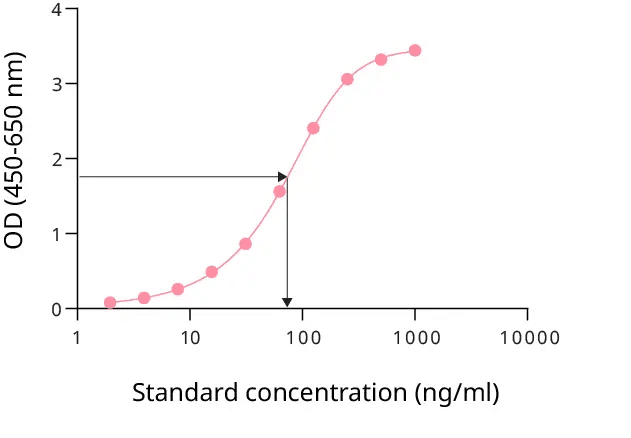
Kết quả ELISA thường được biểu diễn bằng đường chuẩn thể hiện mối quan hệ giữa mật độ quang học (OD) và nồng độ protein mục tiêu đã biết. Đường này được sử dụng để nội suy nồng độ của các mẫu chưa biết, thường được trình bày dưới dạng biểu đồ cột để làm nổi bật sự khác biệt giữa các nhóm thí nghiệm. Dữ liệu phản ánh tổng lượng protein được tiết ra trong mẫu, cung cấp cái nhìn định lượng ở mức tổng thể về sản xuất cytokine hoặc kháng thể.
ELISpot là gì?
ELISpot (Enzyme-Linked ImmunoSpot) là một xét nghiệm miễn dịch có độ nhạy rất cao để đếm các tế bào tiết protein cụ thể, thường là cytokine hoặc kháng thể. Khác với ELISA, đo nồng độ tổng thể của chất phân tích trong mẫu dịch, ELISpot cung cấp cái nhìn chi tiết về đáp ứng miễn dịch ở mức tế bào đơn lẻ. Phương pháp này đặc biệt hữu ích trong nghiên cứu miễn dịch học, nơi việc phát hiện các tế bào T hoặc B đặc hiệu kháng nguyên hiếm là rất quan trọng, chẳng hạn trong phát triển vaccine, nghiên cứu tự miễn hoặc theo dõi liệu pháp miễn dịch ung thư.
Cơ chế hoạt động
Trong ELISpot, các tế bào miễn dịch được thêm vào đĩa PVDF đã được phủ kháng thể bắt giữ đặc hiệu với protein quan tâm. Khi tế bào được kích thích, protein tiết ra sẽ ngay lập tức bị bắt giữ quanh tế bào bởi kháng thể cố định. Sau khi ủ, tế bào được rửa bỏ, và kháng thể phát hiện gắn biotin được thêm vào, tiếp theo là phức hợp streptavidin–enzyme. Sau đó, cơ chất kết tủa được thêm vào, tạo thành các điểm nhìn thấy được tại vị trí các tế bào riêng lẻ đã tiết protein mục tiêu. Mỗi điểm đại diện cho một tế bào đáp ứng và có thể được định lượng bằng máy đọc ELISpot.
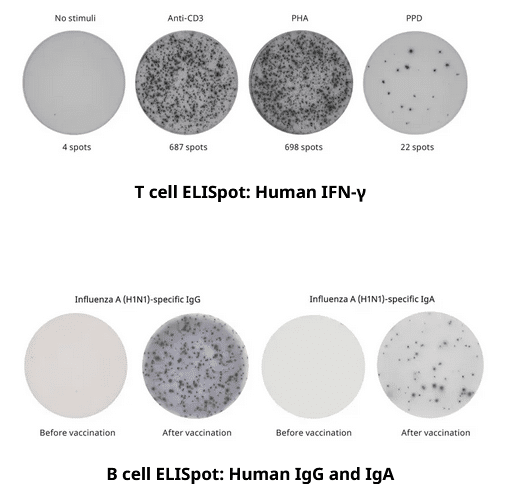
Kết quả ELISpot
Kết quả ELISpot cung cấp số lượng tế bào tiết protein. Mỗi điểm đại diện cho một tế bào đã tiết protein mục tiêu trong quá trình xét nghiệm. Hình ảnh đại diện của các giếng cho thấy các điểm riêng biệt được đếm bằng máy đọc ELISpot. Kết quả thường được trình bày dưới dạng biểu đồ cột thể hiện số đơn vị hình thành điểm (SFU) trên mỗi triệu tế bào, cung cấp độ phân giải ở mức tế bào đơn của hoạt động miễn dịch.
So sánh giữa ELISA và ELISpot
| ELISA | ELISpot | |
|---|---|---|
| Phát hiện | Protein hòa tan | Tế bào tiết protein |
| Loại mẫu | Huyết tương, huyết thanh hoặc dịch nổi | Tế bào sống (ví dụ PBMC) |
| Độ nhạy | Trung bình đến cao (phụ thuộc vào analyte và kit) | Rất cao |
| Kết quả | Nồng độ protein | Số lượng tế bào tiết |
| Cách đọc | Mật độ quang học (OD) bằng máy đọc đĩa | Số điểm bằng máy đọc ELISpot/FluoroSpot |
| Yêu cầu thuốc thử | Cặp kháng thể, thuốc thử phát hiện, chuẩn | Cặp kháng thể, thuốc thử phát hiện |
| Thiết bị | Máy đọc ELISA | Máy đọc ELISpot |
| Khả năng multiplex | Hạn chế (có thể với assay đặc biệt như EYRAplex) | Có thể với FluoroSpot |
| Thông lượng | Cao (định dạng 96 giếng, phù hợp tự động hóa) | Trung bình (xử lý tế bào thủ công là điểm nghẽn) |
| Ưu điểm | Quy trình chuẩn hóa, thiết bị phổ biến | Độ nhạy cao, đọc chức năng, phát hiện đáp ứng hiếm |
| Nhược điểm | Không cho biết số lượng tế bào đáp ứng | Phức tạp hơn, cần tế bào sống và thiết bị chuyên dụng |
| Ứng dụng tốt nhất | Đo mức protein trong dịch | Xác định tế bào tiết cytokine đặc hiệu |
Khi nào nên chọn ELISA
ELISA là lựa chọn phù hợp khi mục tiêu của bạn là định lượng nồng độ của một protein cụ thể trong dung dịch. Dù bạn làm việc với huyết thanh, huyết tương, dịch nổi nuôi cấy tế bào hay các loại dịch khác, ELISA cung cấp một nền tảng đáng tin cậy và đã được thiết lập tốt để phát hiện các chất phân tích hòa tan.
Chọn ELISA khi:
- Bạn cần dữ liệu định lượng (ví dụ: pg/ml hoặc ng/ml).
- Bạn phân tích protein tiết ra như cytokine, kháng thể hoặc hormone.
- Thí nghiệm cần so sánh giữa nhiều mẫu (nhóm điều trị, thời gian).
- Bạn cần giải pháp thông lượng cao, có thể mở rộng và tự động hóa.
- Bạn không có hoặc không cần tế bào miễn dịch sống.
Ứng dụng điển hình:
- Phân tích cytokine sau kích thích.
- Đo hiệu giá kháng thể trong nghiên cứu nhiễm trùng hoặc vaccine.
- Theo dõi biomarker trong mẫu lâm sàng.
- Xác nhận biểu hiện protein trong hệ tái tổ hợp.
Khi nào nên chọn ELISpot
ELISpot là lựa chọn khi bạn cần đánh giá đáp ứng miễn dịch chức năng ở mức tế bào đơn. Phương pháp này được thiết kế để phát hiện và đếm các tế bào riêng lẻ tiết protein mục tiêu, mang lại độ nhạy vượt trội trong việc phát hiện các tế bào đáp ứng hiếm.
Chọn ELISpot khi:
- Bạn cần đo số lượng tế bào tiết protein (ví dụ tế bào T tiết IFN-γ).
- Bạn cần đánh giá miễn dịch qua trung gian tế bào.
- Nghiên cứu liên quan đến vaccine, miễn dịch ung thư hoặc theo dõi tế bào T.
- Bạn làm việc với PBMC hoặc tế bào miễn dịch phân lập.
- Bạn cần độ nhạy rất cao.
Ứng dụng điển hình:
- Theo dõi đáp ứng tế bào T trong thử nghiệm vaccine.
- Đánh giá hoạt hóa miễn dịch trong bệnh truyền nhiễm hoặc ung thư.
- Theo dõi tiết kháng thể của tế bào B ở mức tế bào đơn.
- Phát hiện đáp ứng hiếm không thấy trong phân tích tổng thể.
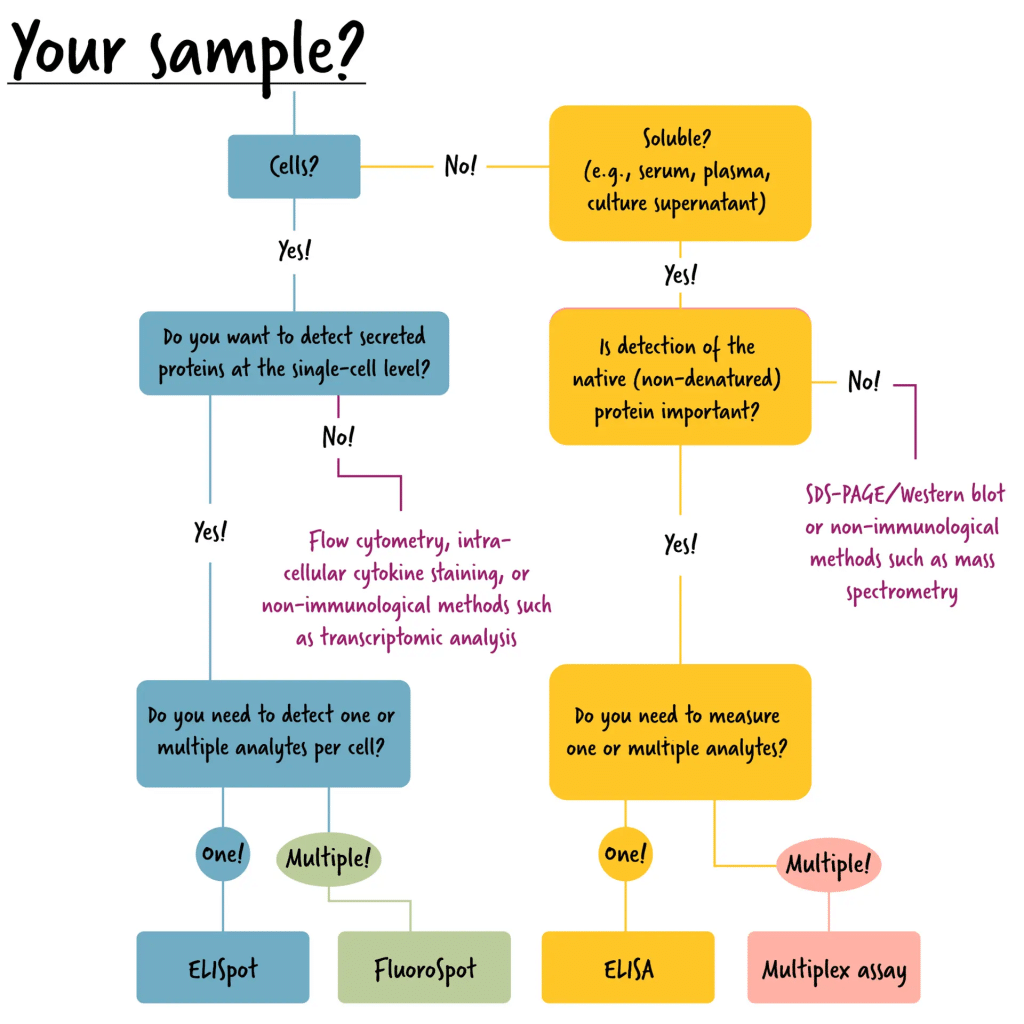
Các yếu tố thực tiễn
Khi lựa chọn giữa ELISA và ELISpot, cần xem xét các yếu tố thực tế của thí nghiệm:
- Loại mẫu
ELISA cần mẫu dạng lỏng (huyết thanh, huyết tương, dịch nổi), phù hợp khi không có tế bào sống. ELISpot cần tế bào miễn dịch tươi hoặc bảo quản đúng cách. - Độ nhạy
ELISpot có độ nhạy rất cao và phát hiện đáp ứng hiếm. ELISA kém nhạy hơn nhưng cung cấp dữ liệu nồng độ đáng tin cậy. - Thiết bị đọc
ELISA dùng máy đọc đĩa phổ biến. ELISpot cần máy chuyên dụng và phần mềm phân tích. - Độ phức tạp
ELISA đơn giản hơn. ELISpot yêu cầu xử lý tế bào cẩn thận. - Kết quả
ELISA cho nồng độ (pg/ml), ELISpot cho số lượng tế bào (SFU/10⁶ tế bào).
Kết hợp ELISA và ELISpot
ELISA và ELISpot có thể bổ trợ lẫn nhau. Ví dụ, ELISpot cho biết bao nhiêu tế bào tạo cytokine, còn ELISA cho biết lượng cytokine trong dịch. Kết hợp hai phương pháp giúp hiểu toàn diện hơn về đáp ứng miễn dịch.
Ví dụ:
- Phát triển vaccine: ELISpot (tế bào T) + ELISA (kháng thể/cytokine)
- Theo dõi miễn dịch: ELISpot (hoạt hóa tế bào) + ELISA (cytokine toàn hệ)
- Tìm biomarker: ELISpot (tế bào hiếm) + ELISA (protein trong dịch)
Kết luận
Cả ELISA và ELISpot đều là công cụ mạnh để đo đáp ứng miễn dịch. ELISA phù hợp để định lượng protein tổng thể trong dịch, trong khi ELISpot cung cấp độ nhạy và độ phân giải ở mức tế bào đơn. Việc lựa chọn phụ thuộc vào câu hỏi nghiên cứu và điều kiện thực tế, tuy nhiên, kết hợp cả hai thường mang lại cái nhìn sâu sắc hơn về hệ miễn dịch.