Khi nói đến điều trị nhiều loại bệnh phức tạp và mạn tính, các thuốc sinh học (biologics) đã thay đổi cuộc chơi nhờ các cơ chế tác động hiệu quả cao như kháng thể đơn dòng (mAbs), liệu pháp miễn dịch và liệu pháp gen (1). Ngay cả khi thị trường biologics tiếp tục mở rộng, những thay đổi lớn đang đến gần. Cụ thể, bằng sáng chế của nhiều thuốc sinh học “bom tấn” với doanh thu hàng năm hơn 200 tỷ USD sẽ hết hạn vào năm 2030, mở ra cơ hội cho sự phát triển của biosimilar (2).
Vậy sự kiện hết hạn bằng sáng chế biosimilar—thường được gọi là “vách đá bằng sáng chế”—sẽ tác động như thế nào đến thị trường dược sinh học? Điều này phụ thuộc vào góc nhìn. Đối với các công ty dược lớn sở hữu các bằng sáng chế này, cạnh tranh có thể gia tăng nhanh chóng, gây rủi ro đáng kể đến doanh thu (3). Ngược lại, các nhà sản xuất nhỏ hơn sẽ có cơ hội sản xuất thuốc biosimilar với chi phí R&D thấp hơn từ 15 đến 20 lần so với thuốc gốc, do các hoạt chất trong sản phẩm đã được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chứng minh về độ an toàn và hiệu quả (4). Nếu bạn là nhà sản xuất muốn phát triển biosimilar nhằm tăng khả năng tiếp cận và giảm chi phí cho bệnh nhân, hãy cân nhắc các chiến lược để tiếp cận thị trường mới này.
Trước hết: Những bằng sáng chế biologic nào sắp hết hạn?
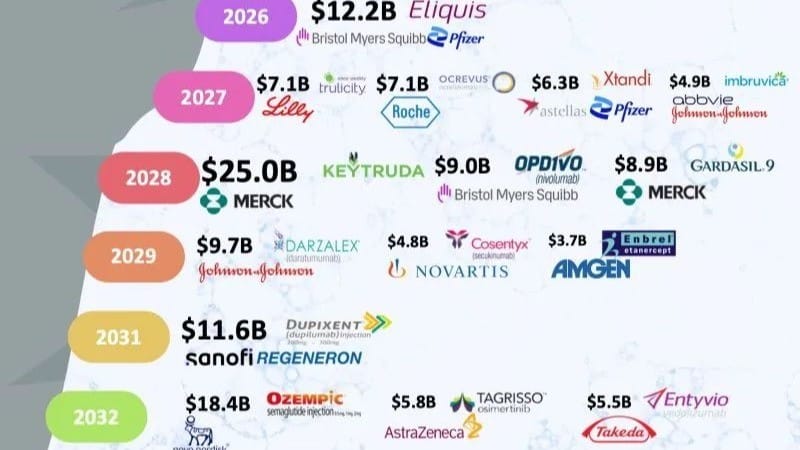
Trước khi xác định loại biosimilar bạn muốn phát triển, hãy tìm hiểu các bằng sáng chế biologic nào đang tiến gần đến thời điểm hết hạn. Dưới đây là danh sách một số bằng sáng chế lớn sẽ hết hạn tại Mỹ trong 5 năm tới (5,6,7).
2025
- Perjeta (pertuzumab), do Genentech sản xuất: điều trị ung thư vú HER2 dương tính
- Benlysta (belimumab), do GSK sản xuất: điều trị lupus ban đỏ hệ thống
- Blincyto (blinatumomab), do Amgen sản xuất: điều trị bệnh bạch cầu lympho cấp
2026
- Kadcyla (ado-trastuzumab emtansine), do Genentech sản xuất: điều trị ung thư vú HER2 dương tính
- Taltz (ixekizumab), do Lilly sản xuất: điều trị vảy nến và viêm khớp vảy nến
- Elelyso (taliglucerase alfa), do Pfizer sản xuất: điều trị bệnh Gaucher
2027
- Myalept (metreleptin), do Amryt Pharmaceuticals sản xuất: điều trị loạn dưỡng mỡ
- Sylvant (siltuximab), do Recordati Rare Diseases sản xuất: điều trị bệnh Castleman
- Trulicity (dulaglutide), do Lilly sản xuất: điều trị đái tháo đường type 2
- Darzalex (daratumumab), do Johnson & Johnson sản xuất: điều trị đa u tủy
2028
- Keytruda (pembrolizumab), do Merck sản xuất: điều trị nhiều loại ung thư
- Opdivo (nivolumab), do Bristol Myers Squibb sản xuất: điều trị nhiều loại ung thư
2029
- Ocrevus (ocrelizumab), do Genentech sản xuất: điều trị đa xơ cứng
Là một nhà phát triển biosimilar, bạn cần thực hiện thẩm định riêng về các bằng sáng chế sắp hết hạn, đồng thời cân nhắc thời điểm, thị trường mục tiêu và năng lực đội ngũ. Để xây dựng chiến lược tốt hơn, hãy xem xét các yêu cầu pháp lý liên quan đến biosimilar.
Biosimilar là gì và lợi ích của chúng?
Theo FDA, biosimilar là một liệu pháp sinh học có độ tương đồng cao nhưng không hoàn toàn giống với một thuốc sinh học đã được FDA phê duyệt (còn gọi là thuốc gốc hoặc sản phẩm tham chiếu) (8). Biosimilar không có khác biệt có ý nghĩa lâm sàng so với thuốc gốc, nghĩa là có cùng độ an toàn, hiệu quả, độ tinh khiết và hoạt lực, và có thể sử dụng thay thế (4).
Tương tự thuốc generic, biosimilar có thể được phê duyệt theo quy trình rút gọn; tuy nhiên, thuốc generic là các phân tử nhỏ được tổng hợp để giống hệt thuốc gốc (5). Vì biologic được tạo ra từ hệ thống sống, nên không thể sao chép hoàn toàn giống nhau, do đó biosimilar không bao giờ được coi là giống hệt sản phẩm tham chiếu (8). Mặc dù có thể tận dụng công nghệ sản xuất và phân tích tiên tiến, biosimilar cần được phát triển sao cho tương đồng tối đa với thuốc gốc để tránh bị phân loại là “biobetter”, điều có thể kéo dài thời gian phát triển (9).
Nhìn chung, biosimilar mang lại các lợi ích như thời gian phát triển nhanh hơn, chi phí thấp hơn, quy trình phê duyệt nhanh hơn và giảm chi phí cho hệ thống y tế, nhà cung cấp và đặc biệt là bệnh nhân (4). Giá biosimilar thường thấp hơn 15–35% so với thuốc biệt dược và đã giúp tiết kiệm gần 13 tỷ USD kể từ năm 2015; dự kiến sẽ tiết kiệm từ 38 đến 124 tỷ USD chi phí y tế trong giai đoạn 2021–2025 (10). Thành công của nhà phát triển biosimilar phụ thuộc lớn vào khả năng triển khai nhanh, lập kế hoạch tốt, xây dựng quan hệ đối tác và tận dụng thế mạnh đội ngũ. Do thị trường cạnh tranh cao, việc phân tích thị trường từ sớm và điều chỉnh chiến lược là yếu tố then chốt.
Các yếu tố thị trường quan trọng trong phát triển biosimilar là gì?
Mặc dù mục tiêu của biosimilar vẫn là tăng khả năng tiếp cận thuốc cứu sống, việc phát triển chúng đi kèm những thách thức riêng. Nhà phát triển cần xác định thị trường mục tiêu ngay từ đầu để đảm bảo tuân thủ quy định liên tục. Một số biosimilar được sản xuất tại khu vực có yêu cầu pháp lý thấp hơn, nhưng việc thâm nhập các thị trường có quy định chặt chẽ như Mỹ có thể mang lại lợi ích tài chính lớn (11).
Do tiềm năng kinh tế lớn, lĩnh vực biosimilar rất cạnh tranh; các nhà phát triển đều cố gắng đưa sản phẩm ra thị trường sớm nhất. Những sản phẩm đầu tiên thường đạt thành công thương mại cao nhất. Vì vậy, cần xác định sản phẩm mục tiêu càng sớm càng tốt để kịp thời gian phát triển rút ngắn (6–9 năm) (4). Đồng thời, cần thực hiện nghiên cứu thị trường và phối hợp với các bên liên quan như bác sĩ và tổ chức bệnh nhân từ giai đoạn sớm (9).
Các yếu tố sản xuất và pháp lý quan trọng trong phát triển biosimilar là gì?
Sau khi xác định sản phẩm và thị trường mục tiêu, cần xây dựng chiến lược phát triển và sản xuất phù hợp. Áp lực đưa sản phẩm ra thị trường nhanh khiến việc sản xuất “right-first-time” trở nên rất quan trọng. Điều này đòi hỏi hiểu rõ phân tử gốc và quy trình sản xuất của nó (12).
Việc kiểm soát chi phí cũng rất quan trọng và cần được đánh giá thông qua các mô hình kinh tế quy trình để lựa chọn chiến lược phù hợp như sản xuất liên tục, hệ thống single-use hoặc thép không gỉ.
Hồ sơ mục tiêu chất lượng (QTPP) của biosimilar dựa trên thuốc gốc. Các thuộc tính chất lượng quan trọng (CQAs) cần tương đồng tối đa. Ví dụ, glycosyl hóa là một CQA quan trọng trong sản xuất mAbs, nên cần đảm bảo sự tương đồng giữa biosimilar và thuốc gốc (14).
Việc xác định các tham số quy trình quan trọng (CPPs) ảnh hưởng đến CQAs là yếu tố then chốt, thường được thực hiện theo phương pháp Quality by Design (QbD). Phân tích tương đồng bằng SPR giúp đánh giá sự tương đồng, kiểm soát chất lượng và tính ổn định giữa các lô sản xuất (13).
Quy trình sản xuất thuốc gốc thường là bí mật, nhưng có thể tham khảo thông tin từ các báo cáo công khai và tài liệu phê duyệt. Đồng thời cần thu thập dữ liệu về cấu trúc và chức năng để hiểu rõ CQAs và tạp chất (15).
Trong suốt quá trình phát triển, cần tuân thủ chặt chẽ các quy định tại thị trường mục tiêu. FDA và EMA đều có hướng dẫn chi tiết cho việc đánh giá biosimilar (15). Do quy định chưa được đồng bộ toàn cầu và thay đổi nhanh, cần cập nhật thường xuyên.
Sau “vách đá bằng sáng chế” sẽ là gì?
Khi phát triển biosimilar sau khi bằng sáng chế hết hạn, cần có chiến lược rõ ràng: đội ngũ phù hợp với loại biologic nào, thị trường nào có nhu cầu cao, và yêu cầu pháp lý ra sao.
Việc hợp tác với đối tác có kinh nghiệm trong phát triển biologic gốc sẽ giúp rút ngắn thời gian, giảm rủi ro, đảm bảo tuân thủ và tăng khả năng thành công thương mại.
Tài liệu tham khảo
- Cleveland Clinic. What are biologics? Cleveland Clinic. https://my.clevelandclinic.org/health/treatments/biologics-biologic-medicine. Updated August 9, 2024. Accessed May 12, 2025.
- Philippidis A. As patent cliff looms for biopharma giants, smaller biotechs face cash crunch. Genetic Engineering and Biotechnology News. https://www.genengnews.com/topics/bioprocessing/as-patent-cliff-looms-for-biopharma-giants-smaller-biotechs-face-cash-crunch/. Published June 21, 2023. Accessed May 12, 2025.
- Gardner J. Big pharma’s looming threat: a patent cliff of “tectonic magnitude.” BioPharma Dive. https://www.biopharmadive.com/news/pharma-patent-cliff-biologic-drugs-humira-keytruda/642660/. Published February 21, 2023. Accessed May 12, 2025.
- Lechleider T. Biosimilars: a cure for the higher price of complex drugs? American Century Investments. https://www.americancentury.com/insights/biosimilars-cure-for-the-higher-price-of-complex-drugs/. Published March 11, 2024. Accessed May 12, 2025.
- Sadowska J. Which biologics are going off patent? LinkedIn. https://www.linkedin.com/feed/update/urn:li:activity:7270421667305181184/. Published 2024. Accessed May 12, 2025.
- GreyB. List – 31 Biologics Coming Off Patents Between 2022 to 2027. GreyB. https://www.greyb.com/blog/biologics-patents-expiring/. Accessed May 12, 2025.
- Burke H. Top 10 drugs with patents due to expire in the next five years. Proclinical. https://www.proclinical.com/blogs/2024-2/top-10-drugs-with-patents-due-to-expire-in-the-next-5-years. Published February 16, 2024. Accessed May 12, 2025.
- United States (US) Food and Drug Administration (FDA). Biosimilars basics for patients. US FDA. https://www.fda.gov/drugs/biosimilars/biosimilars-basics-patients. Published August 1, 2024. Accessed May 12, 2025.
- Carlsen J, Estdale S, Kaiser R, Donninger R, Bower J. Key considerations in biosimilars development. BioPharm International. .https://www.biopharminternational.com/view/key-considerations-biosimilars-development. Published October 1, 2012. Accessed May 12, 2025.
- Feng K, Russo M, Maini L, Kesselheim AS, Rome BN. Patient out-of-pocket costs for biologic drugs after biosimilar competition. JAMA Health Forum. 2024;5(3):e235429. doi:10.1001/jamahealthforum.2023.5429.
- Blackstone EA, Joseph PF. The economics of biosimilars. Am Health Drug Benefits. 2013;6(8): 469-478. https://pmc.ncbi.nlm.nih.gov/articles/PMC4031732/. Accessed May 12, 2025.
- Bui LA, Hurst S, Finch GL, et al. Key considerations in the preclinical development of biosimilars. Drug Discov Today. 2015;20 Suppl 1:3-15. doi:10.1016/j.drudis.2015.03.011.
- Edwards E, Livanos M, Krueger A, et al. Strategies to control therapeutic antibody glycosylation during bioprocessing: synthesis and separation. Biotechnol Bioeng. 2022;119(6):1343-1358. doi:10.1002/bit.28066.
- Vulto AG, Jaquez OA. The process defines the product: what really matters in biosimilar design and production? Rheumatology (Oxford). 2017;56(suppl_4):iv14-iv29. doi:10.1093/rheumatology/kex278.
- Kirchhoff CF, Wang XM, Conlon HD, Anderson S, Ryan AM, Bose A. Biosimilars: key regulatory considerations and similarity assessment tools. Biotechnol Bioeng. 2017;114(12):2696-2705. doi:10.1002/bit.26438.