Sắc ký ái lực có thể được sử dụng để tinh sạch kháng thể từ dịch nuôi cấy tế bào và huyết thanh. Các mảnh kháng thể có thể được tinh sạch nếu chúng chứa vùng tương tác với ligand gắn trên ma trận. Các dạng single-chain variable fragment (scFv), antigen-binding fragment (Fab) và single-domain antibody (dAb) đều có thể được tinh sạch bằng sắc ký ái lực.
Sắc ký ái lực có thể được sử dụng như bước tinh sạch duy nhất cho các ứng dụng không yêu cầu độ tinh sạch cao nhất. Các bước tinh sạch bổ sung có thể cần thiết tùy thuộc vào mục đích sử dụng.
Tại sao tinh sạch kháng thể lại quan trọng trong sản xuất sinh học
Tinh sạch kháng thể là một bước quan trọng trong sản xuất sinh học vì nó cho phép các kháng thể điều trị và các sinh phẩm liên quan đạt được các tiêu chuẩn về độ tinh sạch và chất lượng cần thiết cho tính an toàn và hiệu quả. Trong quá trình sản xuất, nuôi cấy tế bào tạo ra một hỗn hợp phức tạp gồm kháng thể mục tiêu, protein tế bào chủ, DNA, thành phần môi trường và các tạp chất của quy trình. Tinh sạch giúp tách riêng kháng thể mong muốn khỏi hỗn hợp này, thường bắt đầu bằng bước thu nhận ái lực có độ chọn lọc cao để làm giàu phân tử mục tiêu và giảm tạp chất. Các bước tinh sạch tiếp theo được sử dụng để loại bỏ các dạng kết tụ, mảnh vỡ và tạp chất vết có thể ảnh hưởng đến độ ổn định, hoạt lực hoặc tính sinh miễn dịch. Việc tinh sạch hiệu quả không chỉ cải thiện tính đồng nhất của sản phẩm và khả năng sản xuất downstream mà còn giúp đáp ứng các yêu cầu tuân thủ quy định, khiến nó trở thành một phần thiết yếu trong sản xuất các liệu pháp kháng thể đáng tin cậy.
Tinh sạch kháng thể là gì?
Tinh sạch kháng thể là quá trình phân lập kháng thể từ các hỗn hợp sinh học phức tạp, như huyết thanh, dịch cổ trướng hoặc dịch nổi nuôi cấy tế bào, nhằm thu được vật liệu đủ tinh sạch cho nghiên cứu, phát triển liệu pháp hoặc xét nghiệm chẩn đoán.
Kháng thể đa dòng, kháng thể đơn dòng (mAb) và các mảnh kháng thể thường được tinh sạch bằng sắc ký ái lực. Các resin chứa ligand cố định (ví dụ: Protein A, Protein G hoặc Protein L) được sử dụng để bắt giữ kháng thể và các mảnh kháng thể.
Tinh sạch ái lực mang lại độ chọn lọc cao. Mức độ tinh sạch trên 95% thường có thể đạt được chỉ trong một bước. Tuy nhiên, nhiều ứng dụng của kháng thể sẽ yêu cầu tinh sạch thêm. Sắc ký lọc gel (size exclusion chromatography) thường được chọn cho bước “polishing” để tách monomer khỏi các dạng kết tụ.
Khám phá cách các resin sắc ký cho phép tách chọn lọc kháng thể khỏi các hỗn hợp phức tạp. Tìm hiểu thêm về các loại resin sắc ký khác nhau được sử dụng cho tinh sạch kháng thể tại đây.
Tổng quan quy trình tinh sạch kháng thể
Sắc ký ái lực kháng thể, như trình bày trong Hình 1, dựa trên ái lực và tính đặc hiệu cao của Protein A và Protein G đối với vùng Fc của IgG từ nhiều loài. Protein L, liên kết với chuỗi nhẹ kappa, là một ligand khác có thể được sử dụng để tinh sạch các mảnh kháng thể, IgG và các kháng thể khác từ nhiều loài sinh vật nhân thực.
Sự gắn kết giữa kháng thể và ligand là thuận nghịch, và kháng thể thường được rửa giải bằng cách giảm pH.
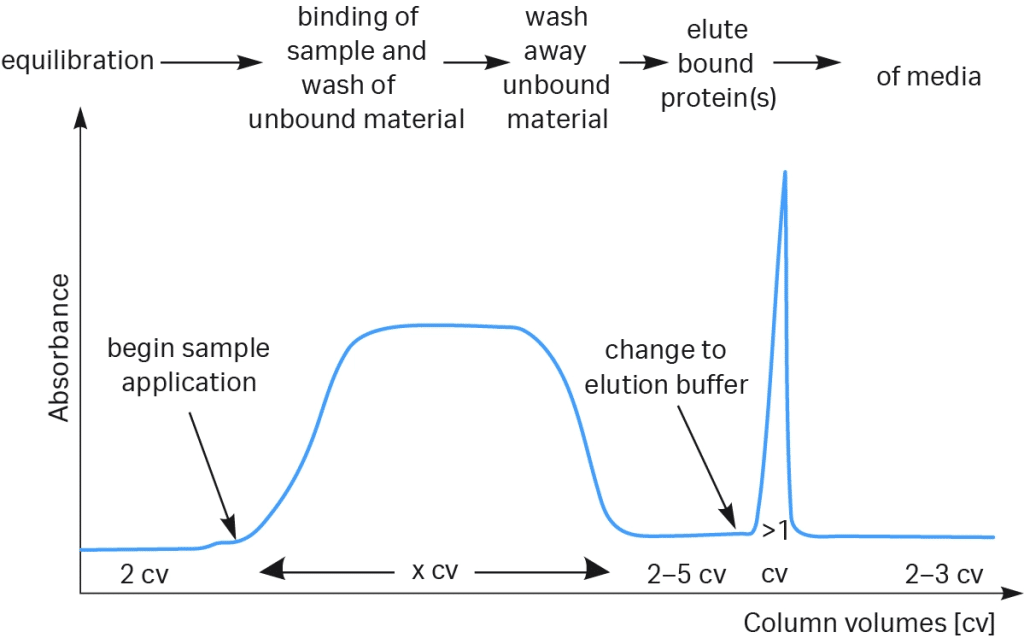
Các bước capture, intermediate và polishing
Các bước capture, intermediate và polishing tạo thành một cách tiếp cận theo từng giai đoạn để tinh sạch kháng thể, giúp tăng dần độ tinh sạch và loại bỏ các nhóm tạp chất khác nhau. Bước capture thường là bước sắc ký đầu tiên, sử dụng các resin ái lực có độ chọn lọc cao như Protein A để tách kháng thể mục tiêu khỏi hỗn hợp phức tạp và loại bỏ phần lớn protein tế bào chủ và mảnh vụn. Bước intermediate tiếp theo nhằm giảm các tạp chất liên quan đến quy trình như DNA, endotoxin, Protein A bị rò rỉ và các thành phần môi trường còn sót lại, đồng thời bắt đầu tinh chỉnh hồ sơ phân tử của kháng thể. Cuối cùng, các bước polishing, thường sử dụng sắc ký trao đổi ion hoặc sắc ký lọc gel, được dùng để loại bỏ các dạng kết tụ, mảnh vỡ và tạp chất vết có thể ảnh hưởng đến độ ổn định, hoạt lực hoặc độ an toàn. Tổng thể, các giai đoạn này cung cấp một lộ trình có hệ thống để đạt được độ tinh sạch và tính nhất quán cần thiết cho sản xuất kháng thể cấp độ điều trị.
Các loại kháng thể và ảnh hưởng đến chiến lược tinh sạch
Các loại kháng thể khác nhau, như kháng thể đa dòng, kháng thể đơn dòng, các mảnh kháng thể và các dạng thiết kế (engineered), có thể định hình chiến lược tinh sạch vì mỗi phân tử tương tác khác nhau với các resin sắc ký thông dụng và có thể yêu cầu các điều kiện tối ưu riêng để đạt độ tinh sạch cao. Kháng thể đơn dòng IgG toàn phần thường liên kết tốt với Protein A, giúp bước capture ái lực hiệu quả và dễ dự đoán, trong khi các mảnh kháng thể như Fab hoặc scFv thường có ái lực với Protein A thấp hoặc không có, và có thể cần Protein L, Protein G hoặc các hóa học bắt giữ thay thế. Kháng thể đa dòng, là hỗn hợp không đồng nhất của nhiều loại kháng thể, có thể yêu cầu các resin có độ chọn lọc rộng hơn hoặc các bước intermediate bổ sung để loại bỏ các quần thể biến thể và tạp chất có nguồn gốc từ tế bào chủ. Các kháng thể thiết kế, như kháng thể hai đặc hiệu hoặc các cấu trúc biến đổi Fc, cũng có thể đặt ra những thách thức riêng, bao gồm thay đổi khả năng liên kết với ligand ái lực hoặc xu hướng kết tụ cao hơn, điều này ảnh hưởng đến yêu cầu của bước polishing. Những khác biệt phân tử này định hướng lựa chọn ligand cho bước capture, xác định mức độ loại bỏ tạp chất cần thiết ở bước intermediate và định hình chiến lược polishing để sản phẩm cuối cùng đáp ứng các yêu cầu về độ tinh sạch và độ ổn định cấp điều trị.
Tinh sạch kháng thể đơn dòng
Tinh sạch kháng thể đơn dòng là quá trình phân lập một loài kháng thể duy nhất, được xác định rõ, từ dịch thu hoạch nuôi cấy tế bào phức tạp và loại bỏ các tạp chất tích tụ trong quá trình sản xuất. Do các kháng thể IgG đơn dòng toàn phần liên kết mạnh và đặc hiệu với Protein A, quá trình tinh sạch thường bắt đầu bằng bước capture ái lực để làm giàu phân tử mục tiêu và loại bỏ phần lớn protein tế bào chủ và mảnh vụn chỉ trong một thao tác. Sau đó là các giai đoạn intermediate và polishing nhằm tinh chỉnh chất lượng phân tử, loại bỏ các dạng kết tụ, mảnh vỡ, DNA, endotoxin và các tạp chất vết khác có thể ảnh hưởng đến độ ổn định hoặc hiệu năng. Tổng thể, các bước này cung cấp một quy trình kiểm soát và hiệu quả để đạt được độ tinh sạch cao, tính nhất quán và chất lượng đạt chuẩn quy định cần thiết cho các sản phẩm kháng thể đơn dòng điều trị.
Tinh sạch kháng thể đa dòng
Tinh sạch kháng thể đa dòng là quá trình phân lập một hỗn hợp đa dạng các loại kháng thể được tạo ra bởi động vật đã được gây miễn dịch và loại bỏ các tạp chất đi kèm có trong huyết thanh hoặc huyết tương. Do kháng thể đa dòng có sự khác biệt về trình tự và cấu trúc, chúng không liên kết đồng đều với một ligand ái lực duy nhất, vì vậy quá trình tinh sạch thường bắt đầu với các phương pháp capture có độ chọn lọc rộng hơn như Protein A, Protein G hoặc các resin mixed-mode để làm giàu quần thể Ig mong muốn và loại bỏ protein khối lượng lớn. Các bước intermediate sau đó được sử dụng để giảm các thành phần có nguồn gốc từ cơ thể như albumin, lipid và protease đồng thời làm chặt chẽ hồ sơ phân tử tổng thể. Các bước polishing cuối cùng loại bỏ các dạng kết tụ còn lại, tạp chất hàm lượng thấp và tạp chất quy trình có thể ảnh hưởng đến độ ổn định hoặc hiệu năng. Tổng thể, các bước này tạo ra một lộ trình hiệu quả để đạt được các chế phẩm kháng thể đa dòng có chất lượng cao và ổn định, phù hợp cho nghiên cứu, chẩn đoán hoặc điều trị.
Các kỹ thuật sắc ký cốt lõi cho tinh sạch kháng thể

Các kỹ thuật sắc ký cốt lõi cho tinh sạch kháng thể khai thác sự khác biệt về ái lực phân tử, điện tích, tính kỵ nước và kích thước để tách dần kháng thể mục tiêu khỏi tạp chất. Các phương pháp bổ trợ này cùng nhau cho phép sản xuất các sản phẩm kháng thể có độ tinh sạch cao và tính nhất quán trên nhiều định dạng và ứng dụng khác nhau.
- Sắc ký ái lực: Thường sử dụng resin Protein A, Protein G hoặc Protein L để gắn chọn lọc immunoglobulin và loại bỏ phần lớn tạp chất trong một bước capture.
- Sắc ký trao đổi ion: Áp dụng trong các giai đoạn intermediate hoặc polishing để tách các phân tử theo điện tích và loại bỏ protein tế bào chủ, ligand bị rò rỉ và các tạp chất liên quan đến quy trình.
- Sắc ký tương tác kỵ nước: Phân giải các biến thể gần giống nhau hoặc các dạng kết tụ dựa trên sự khác biệt về tính kỵ nước bề mặt.
- Sắc ký lọc gel: Cung cấp khả năng phân tách theo kích thước với độ phân giải cao, lý tưởng để loại bỏ các dạng kết tụ, mảnh vỡ và các tạp chất theo kích thước phân tử.
Các thách thức chính trong tinh sạch kháng thể
Các thách thức chính trong tinh sạch kháng thể xuất phát từ sự đa dạng của tạp chất, các biến thể phân tử và các tạp chất liên quan đến quy trình cần được loại bỏ mà không làm ảnh hưởng đến chất lượng hoặc hiệu suất thu hồi sản phẩm. Khi các định dạng kháng thể phát triển, các phương pháp tinh sạch phải theo kịp với sự thay đổi về hành vi liên kết, xu hướng kết tụ và hồ sơ tạp chất.
- Kháng thể thường tồn tại cùng với protein tế bào chủ, DNA, lipid và các thành phần môi trường, vốn khó tách do có tính chất vật lý hoặc hóa học tương đồng.
- Các biến thể phân tử—bao gồm dạng kết tụ, mảnh vỡ, các isoform điện tích và các chuỗi ghép sai—đòi hỏi các bước phân tách có độ phân giải cao nhưng vẫn đảm bảo thông lượng và khả năng mở rộng.
- Các resin ái lực như Protein A có thể gây ra các thách thức như rò rỉ ligand hoặc độ ổn định hạn chế dưới điều kiện làm sạch khắc nghiệt.
- Các kỹ thuật downstream phải cân bằng giữa mục tiêu độ tinh sạch với dung lượng resin, tính tương thích của buffer, độ bền quy trình và chi phí.
- Các định dạng kháng thể mới (ví dụ: bispecific, phân tử biến đổi Fc và các mảnh kháng thể) yêu cầu chiến lược tinh sạch linh hoạt do hành vi thay đổi và các mẫu tạp chất đặc thù.
Lựa chọn và tối ưu hóa resin sắc ký
Việc lựa chọn và tối ưu hóa resin sắc ký tập trung vào việc phù hợp hóa học resin, dung lượng gắn kết và độ bền với loại kháng thể và hồ sơ tạp chất cụ thể, đảm bảo mỗi bước tinh sạch đạt được độ chọn lọc và hiệu quả cần thiết trong khi vẫn duy trì hiệu suất tổng thể của quy trình. Lựa chọn resin ái lực phù hợp, chẳng hạn vật liệu Protein A có dung lượng cao cho kháng thể đơn dòng, đặt nền tảng cho bước capture hiệu quả, trong khi các resin trao đổi ion, tương tác kỵ nước và lọc gel được đánh giá cho các giai đoạn intermediate và polishing dựa trên khả năng phân giải các dạng kết tụ, biến thể và các tạp chất tương tự mà không làm giảm hiệu suất thu hồi hoặc khả năng mở rộng. Việc tối ưu hóa tập trung vào tinh chỉnh các tham số vận hành như mật độ nạp mẫu, tốc độ dòng, thành phần buffer và điều kiện làm sạch nhằm cân bằng giữa độ tinh sạch, thông lượng và tuổi thọ resin. Tổng thể, các quyết định này định hình một quy trình tinh sạch vừa bền vững về mặt kỹ thuật vừa thích ứng với các định dạng kháng thể đang phát triển.
Các cân nhắc về scale-up và phát triển quy trình
Việc scale-up và phát triển quy trình tinh sạch kháng thể đòi hỏi cân bằng giữa hiệu suất ở quy mô phòng thí nghiệm và các yêu cầu thực tế của sản xuất, đảm bảo các bước sắc ký vẫn hiệu quả, có thể tái lập và khả thi về kinh tế ở quy mô lớn hơn. Khi quy trình chuyển từ cột nhỏ sang quy mô pilot và sản xuất, các yếu tố như kích thước cột, phân bố dòng, giới hạn áp suất và độ nén resin phải được đánh giá cẩn thận để duy trì dung lượng gắn kết và độ phân giải. Việc chuẩn bị và vận chuyển buffer cũng trở nên phức tạp hơn, đòi hỏi tối ưu hóa thể tích buffer, thời gian lưu trữ và chiến lược trộn để đảm bảo vận hành ổn định. Ngoài ra, tuổi thọ resin, quy trình làm sạch và lịch trình chu kỳ phải được tinh chỉnh để duy trì thông lượng trong khi kiểm soát chi phí. Tổng thể, các yếu tố này định hướng phát triển các quy trình tinh sạch có thể mở rộng mượt mà, duy trì chất lượng sản phẩm và hỗ trợ sản xuất sinh học công suất cao, bền vững.
Kết luận
Những yếu tố trên cho thấy việc tinh sạch kháng thể thành công phụ thuộc vào sự kết hợp giữa lựa chọn resin phù hợp, tối ưu hóa từng bước và chiến lược scale-up hợp lý để đáp ứng các yêu cầu của sản xuất sinh học hiện đại. Lựa chọn các resin có độ chọn lọc, dung lượng và độ bền phù hợp tạo nền tảng cho hiệu suất tách ổn định, trong khi các điều kiện vận hành được tinh chỉnh đảm bảo mỗi giai đoạn đóng góp vào độ tinh sạch và hiệu suất thu hồi cao mà không ảnh hưởng đến thông lượng hoặc độ ổn định quy trình. Khi quy trình chuyển từ phát triển sang sản xuất, việc chú ý đến thiết kế cột, quản lý buffer và tuổi thọ resin trở nên thiết yếu để duy trì hiệu quả và tính kinh tế. Bằng cách tích hợp các yếu tố này vào một chiến lược thống nhất, các nhà phát triển có thể xây dựng các quy trình tinh sạch vừa thích ứng với các định dạng kháng thể mới vừa đảm bảo cung cấp ổn định các sản phẩm điều trị chất lượng cao.
Câu hỏi thường gặp (FAQs)
Làm thế nào để chọn resin sắc ký phù hợp cho kháng thể của tôi?
Chọn resin sắc ký bằng cách ghép ligand (Protein A, G hoặc L) với vùng liên kết cụ thể, loài và định dạng của kháng thể—IgG toàn phần thường gắn với Protein A hoặc G, trong khi các mảnh không có vùng Fc cần Protein L.
Isotype kháng thể ảnh hưởng như thế nào đến hiệu quả gắn kết với Protein A?
Hiệu quả gắn kết với Protein A thay đổi theo isotype vì các phân lớp IgG và loài khác nhau có ái lực khác nhau với ligand Protein A. IgG1, IgG2 và IgG4 của người gắn mạnh, trong khi IgA, IgD và IgE gắn yếu hoặc không gắn.
Phương pháp tốt nhất để tinh sạch kháng thể đơn dòng ở quy mô lớn là gì?
Sắc ký ái lực Protein A là phương pháp tốt nhất, cung cấp độ chọn lọc cao và liên kết mạnh với IgG, là tiêu chuẩn công nghiệp cho bước capture.
Tại sao sắc ký Protein A là tiêu chuẩn cho tinh sạch kháng thể đơn dòng?
Vì Protein A gắn mạnh và chọn lọc với vùng Fc của IgG, cho phép thu nhận hiệu quả với độ tinh sạch cao chỉ trong một bước.
Tinh sạch kháng thể đa dòng khác gì so với đơn dòng?
Kháng thể đa dòng là hỗn hợp không đồng nhất, thường cần resin có độ chọn lọc rộng hơn và nhiều bước hơn để loại bỏ tạp chất, trong khi kháng thể đơn dòng có thể tinh sạch hiệu quả bằng quy trình Protein A chuẩn hóa.
Những yếu tố nào ảnh hưởng đến độ tinh sạch và hiệu suất thu hồi trong tinh sạch kháng thể đa dòng?
Độ tinh sạch và hiệu suất phụ thuộc vào bản thân kháng thể; các bước như kết tủa muối hoặc chọn lọc ái lực có thể làm giàu hoặc gây mất mẫu tùy vào mức độ chọn lọc khi loại bỏ tạp chất.